罗沙司他(FG-4592)胶囊是一种可口服的强效可逆性低氧诱导因子脯氨酰羟化酶抑制剂,能够短暂稳定并激活HIF转录因子,启动适应性转录反应,从而在含氧量正常的条件下,模拟了在人体低氧环境下才发生的促红细胞的生成反应,包括产生内源性促红细胞生成素以及通过减少铁调素进行铁动员,最终诱导红细胞生成,改善贫血。
罗沙司他已在欧盟(EU)成员国(包括欧洲经济区(EEA)国家)以及日本、中国、智利和韩国获批用于治疗接受透析(DD)和未接受透析(NDD)的慢性肾病(Chronic kidney disease,CKD)成人贫血患者。
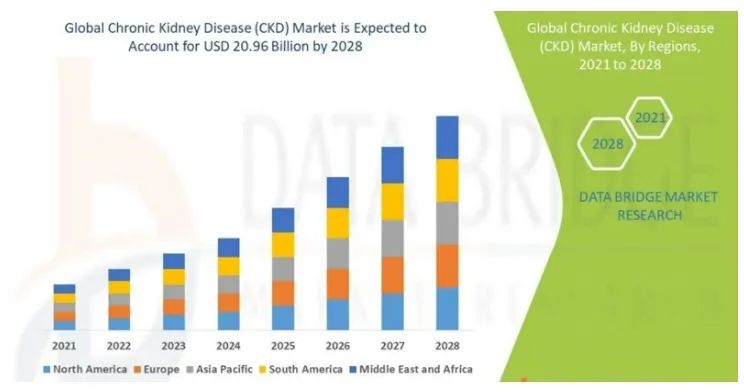
慢性肾脏病(CKD)正以显著的发病率和死亡率威胁人类健康,全球患病率平均为13.4% (总患病率介于11.7–15.1%之间) ,且呈逐年增加趋势。2020年中国成年人群患病人数已达1.38亿人。
据专业分析显示,在2021-2028年的预期内,全球慢性肾脏病(CKD)用药市场将以5%的潜在增长率增长,预计到2028 年将达到209.6亿美元规模。
肾性贫血为慢性肾脏病(CKD)肾功能失代偿期主要并发症之一,随着CKD的进展,CKD相关贫血的患病率和严重程度逐渐增加。根据欧美数据,预期的贫血率为:血液透析(HD)患者>95%,腹膜透析(PD)患者>80%。透析前,3期非透析患者贫血率为10%,4期非透析患者贫血率为>50%,5期非透析患者贫血率为>75%。
我国约有9500万CKD患者,每年约30万CKD患者进展至终末期肾病(ESRD),其中大部分人患有贫血。
化疗性贫血在II期临床研究中取得积极结果,在全球范围开发和商业化
罗沙司他是一种口服药物,是HIF-PH抑制剂类新药中的第一款成药,通过增加内源性促红细胞生成素的生成、改善铁的吸收和调动并降低铁调素,以促进红细胞生成。同时,罗沙司他用于慢性肾脏病(CKD)贫血和骨髓增生异常综合征(MDS)相关贫血的治疗的临床开发也正在进行中。据官方披露,安斯泰来和阿斯利康已向全球监管机构提交了罗沙司他的其他几项许可申请,目前正在审批中。
在去年8月25日— 罗沙司他的原研开发商,美国珐博进公司,宣布其首创作用机制口服小分子低氧诱导因子脯氨酰羟化酶抑制剂罗沙司他,在用于治疗化疗引起的贫血(CIA)的II期临床研究WHITNEY中取得积极的结果。
WHITNEY是一项II期、开放标签研究,旨在研究罗沙司他用于治疗正在接受化疗的非髓性恶性肿瘤患者的贫血的有效性和安全性。该研究主要有效性终点,即在未输注红细胞的情况下,16周内血红蛋白相对于基线的最大变化值,达到了预期指标。
“化疗引起的贫血使许多癌症患者的治疗变得复杂,罗沙司他是一种具有前景的治疗化疗引起的贫血的新方法,”珐博进首席医学官表示,“有必要开展进一步研究,以评价罗沙司他是否能够有效、安全地治疗这一重要类型的贫血。”
在WHITNEY研究项目中,共入组了92例血红蛋白水平≤ 10 g/dL的非髓性恶性肿瘤(实体瘤)患者。患者接受的罗沙司他起始剂量为2.0 mg/kg或2.5 mg/kg,每周三次(TIW),治疗期为16周,另有4周随访期。可每4周滴定一次剂量。
该研究结果表明,罗沙司他的耐受性良好,不同起始剂量组之间的治疗中出现的不良事件(TEAE)无实质性差异。
化疗引起的贫血(CIA)是化疗最常见的副作用之一,却通常未被意识到,且经常治疗不足。CIA可对患者的长期结局产生不利影响,因为贫血限制了生活质量和化疗的有效性。CIA的发病率和严重程度取决于多种因素,包括癌症类型和治疗方案,如化疗类型、时间进度和治疗强度,也取决于患者既往是否接受过骨髓抑制化疗、放疗或两者兼有。估计30%-90%接受化疗的癌症患者会发生贫血。在美国,每年约有65万癌症患者接受化疗。
由于肿瘤本身及治疗过程中均可导致贫血,因此,肿瘤患者贫血的发生率高达50%。在晚期和接受化疗或放疗的患者中贫血发生率可超过90%。
根据2012年中国有关癌性贫血的相关数据,中国癌性贫血的发病率高达60.83%,与欧洲基本持平(63.4%),但治疗率却仅为6.9%,与欧洲相差甚远(38.9%)
据珐博进透露,其已与安斯泰来合作于日本、欧洲、土耳其、俄罗斯和独立国家联合体、中东和南非地区进行罗沙司他用于贫血潜在治疗的开发和商业化。同时在美国、中国、其他美洲市场、澳大利亚/新西兰和东南亚地区也同步进行罗沙司他用于贫血潜在治疗的开发和商业化。
罗沙司他市场潜能巨大,已有企业瞄准,攻破晶型专利提前9年上市
罗沙司他是由阿斯利康和珐博进合作开发的全球首个口服低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),为全球首个同步研发的1类新药。2018年12月,被列入我国“重大新药创制” 科技重大专项的罗沙司他获批于我国上市,可用于慢性肾脏病透析患者贫血的治疗,包括血液透析和腹膜透析患者。此外,值得关注的是罗沙司他还为首个在中国获批上市的肾性贫血口服新药,可用于透析患者治疗的肾性贫血治疗,市场潜能巨大。
今年8月,华威医药官宣,收到国家知识产权局复审与无效审理部针对专利201710546354.X的无效宣告案件作出的第57543号无效决定,正式宣告其专利权全部无效。
罗沙司他胶囊的化合物专利于2024年届满,晶型专利2033年届满,华威表示,如果能把晶型专利无效,仿制药上市时间将可以提前9年。最后,华威对罗沙司他的晶型专利无效挑战成功,主要依据为:
1.已上市的罗沙司他胶囊采用的晶型即专利201710546354.X中所保护的晶体形态。
2.该专利权利要求1-6不具备创造性。
罗沙司他胶囊在国内于2018-12-17获批,2019年底进医保,在2020年有4.5亿元的销售额,2021年国内销售规模已超12亿元,2022年前二季度已录得5亿元以上的销售数据。
另外,据业内统计,截至 2021年6月底,罗沙司他已经覆盖了国内约 81% 具有治疗慢性肾病贫血的相关医院市场。






